Microbiote et endométriose : des liens étroits à double sens
Si, depuis quelques temps, de nombreuses études présentent de fortes preuves sur le lien entre perturbation du microbiote intestinal (dysbiose) et certaines maladies inflammatoires, maladies neuropsychiatriques, psoriasis, arthrite ou cancers, il a été récemment démontré qu’une dysbiose dans l’appareil génital féminin ou dans le microbiome intestinal pourrait être associé à l’endométriose[1]. Qu’est-ce que le microbiote ? Quel rôle joue-t-il dans le corps humain ? Comment peut-il avoir un lien avec l’endométriose ? Explications.
Sommaire
ToggleQu’est-ce que le microbiote ?
Définition générale du microbiote
Le microbiote correspond à l’ensemble des micro-organismes (bactéries, virus, champignons/levures, archées, etc.) peuplant un microbiome. On parle aussi de la « flore ».
On retrouve le microbiote à différents endroits du corps humain :
- dans le tube digestif : le microbiote intestinal
- au niveau des organes génitaux : le microbiote vaginal, avec de nombreux lactobacilles favorisant l’acidité du vagin mais aussi le microbiote utérin ;
- mais aussi sur la peau, dans la bouche ou dans les voies respiratoires…
L’équilibre de ces écosystèmes peut être altéré (antibiotiques, bain de bouche antibactérien, par des savons) et la destruction de bactéries du microbiote peut favoriser la prolifération de la levure Candida, responsable de mycoses.
Focus sur le microbiote intestinal, le microbiote vaginal et le microbiote utérin
Le microbiote intestinal, appelé aussi flore intestinale
Le microbiote intestinal (ou flore intestinale) est constitué d’un ensemble de bactéries, virus, parasites et champignons non pathogènes. Ainsi dans le tube digestif (intestin grêle et colon) de l’être humain, on retrouve 1012 à 1014 micro-organismes, soit 2 à 10 fois plus que le nombre de cellules qui constituent notre corps. Cela représente 2 kilogrammes de micro-organismes.
Le microbiote intestinal joue un important rôle dans les fonctions digestive, métabolique, immunitaire et neurologique. Par conséquent, la dysbiose (l’altération de la flore intestinale), est une piste sérieuse pour comprendre l’origine de certaines maladies, notamment celles sous-tendues par des mécanismes auto-immuns ou inflammatoires (deux caractéristiques de l’endométriose…).
Le microbiote de l’appareil génital féminin : focus sur le vagin, l’utérus et l’endomètre
Les différents organes de l’appareil reproducteur féminin ne sont pas stériles : tant le vagin, que l’utérus/endomètre, le col de l’utérus, les trompes de Fallope ou le liquide péritonéal sont composés d’un microbiote spécifique avec différents types de bactéries. Leur flore est issue naturellement de la flore intestinale, vésicale (de la vessie) et vaginale, donc aussi en lien avec le microbiote du partenaire actuel et des partenaires passés.
Le vagin et l’utérus sont dominés par la souche de bactéries Lactobacillus (L. crispatus, L. iners et autres Lactobacillus spp). Au niveau de l’endomètre, on retrouve d’autres types de bactéries : Pseudomonas, Acinetobacter, Vagococcus et Sphingobium. Leurs proportions augmentent jusqu’au niveau des trompes de Fallope[2].
Les bactéries observées chez une même femme évoluent en fonction du cycle menstruel et de la présence – ou non – de pathologies gynécologiques (tumeurs utérines bénignes, adénomyose, infertilité due à une endométriose)[3]. Ainsi, dans l’utérus par exemple, la flore évolue en fonction des hormones (œstrogène et progestérone) mais aussi avec les menstruations qui, en éliminant l’endomètre, et en permettant de le reconstituer complètement à chaque cycle remet les compteurs à zéro, au moins partiellement, tous les mois. On comprend alors facilement que l’état du microbiote peut être un bon indicateur de différentes pathologies et notamment de la présence d’endométriose, mais aussi de fibromes, etc.
Microbiote et endométriose : en quoi sont-ils liés ?
De plus en plus d’études évoquent un lien probable entre endométriose et microbiote intestinal et génital. Une étude qui date de 2019[4] a notamment démontré qu’une altération du microbiote dans l’appareil génital féminin ou dans le microbiome intestinal pourrait être associé à l’endométriose. Cela s’explique par la potentielle fonction immuno-régulatrice du microbiote intestinal et du microbiote génital qui jouent tous les deux un rôle dans les réponses cellulaires inflammatoires systémiques.

Un guide accessible et digeste afin de vous informer sur ce symptôme très peu abordé par la médecine allopathique et complémentaire :
- de nombreuses clés de compréhension de ce symptôme multifactoriel
- une feuille de route pour agir dès aujourd’hui grâce à des outils simples et efficaces
Le guide de l’Endobelly : En comprendre les causes et agir pour se réconcilier avec son ventre
Vous avez déjà ressenti un ou plusieurs de ces symptômes :
- Gonflement important du ventre
- Ventre dur
- Ventre douloureux ou inconfortable
- Ballonnements
- Perte d’appétit
- Nausées
- Crampes abdominales
- Constipation
- Diarrhées
- Mouvements intestinaux douloureux
- Vertiges
- Vomissements
Plusieurs jours par mois, vous ne savez plus comment vous habiller car soit vos vêtements sont très inconfortables, soit ils sont tout simplement impossibles à enfiler.
On vous a déjà demandé si vous étiez enceinte de 4 voire 6 mois alors que vous étiez malheureusement en pleine crise d’endométriose ou d’endobelly.
Vous n’avez pas été prise au sérieux par les experts à qui vous avez parlé de ce symptôme que vous reliez à l’endométriose, qui est souvent peu reconnu et pour lequel il n’y a soi-disant pas de solution.
Le rôle du microbiote dans l’immunité et le développement de l’endométriose
L’endométriose est une maladie chronique systémique avec plusieurs composantes : hormonale et gynécologique notamment mais aussi inflammatoire et immunitaire (voir le livre du professeur Charles Chapron, chef du service Gynécologie obstétrique et médecine de la reproduction de l’hôpital Cochin à Paris.
En effet, même si l’origine de l’endométriose n’est pas encore unanimement partagée dans le monde scientifique, l’installation, le développement et la progression des lésions d’endométriose sur les différents organes du corps féminin est rendue possible par une réponse immunitaire est altérée, car en temps normal, le système immunitaire ne permet pas à des cellules de se développer dans des zones anormales. Par ailleurs, des études ont montré chez les femmes atteintes d’endométriose une plus forte production d’anticorps de nature auto-immune et une baisse des de l’activité des cellules tueuses naturelles (natural killer cells) surtout dans les stades avancés de l’endométriose.
Cette composante immunitaire est particulièrement intéressante dans le cadre du rôle que le microbiote joue sur la maladie et son développement. Le système immunitaire de la femme atteinte de la maladie est en permanence en train d’essayer de supprimer les lésions (qui sont considérées comme des envahisseurs par les cellules immunitaires) mais sans succès, ce qui va causer de l’inflammation chronique et potentiellement endommager les différents microbiotes qui eux-mêmes jouent un rôle fondamental dans l’immunité humaine. Le cercle vicieux est enclenché.
| Focus sur le lien entre microbiote et système immunitaire 70 % des cellules immunitaires du corps humain sont situées dans l’intestin. Cet organe, et plus particulièrement les bactéries qu’il contient (microbiote), joue un rôle majeur de défense contre les agents pathogènes. Préserver l’intégrité du microbiote intestinal est essentiel pour maintenir de bonnes défenses immunitaires car un microbiote en bon état joue un rôle de barrière contre les micro-organismes pathogènes et il a un effet stimulant sur les cellules immunitaires intestinales. 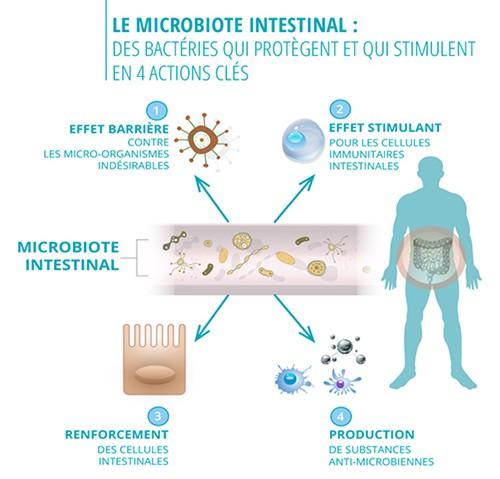 Source : Laboratoire Lescuyer |
Puisque la réponse inflammatoire anormale et l’activation des cellules immunitaires dans la cavité péritonéale sont considérées comme jouant un rôle dans l’émergence et le développement de l’endométriose, une association entre microbiote et endométriose semble être probable.
Il est plausible que le microbiote intestinal joue un rôle dans le développement de l’endométriose en affectant les fonctions biochimiques, immunologiques et épigénétiques de la femme atteinte de la maladie.
Et le lien entre microbiote et endométriose serait encore plus complexe car il faudrait également tenir compte du microbiote génital (vaginal et utérin notamment). En comparant les microbiotes intestinal, vaginal et utérin de femmes atteintes d’endométriose et de femmes non atteintes de cette pathologie, plusieurs conclusions sont apparues :
- l’absence complète des bactéries Atopobium dans le microbiote vaginal et cervical pour les femmes atteintes d’endométriose de stade 3 et 4 a été remarqué
- dans le microbiote du col de l’utérus, les bactéries Gardnerella, Streptococcus, Escherichia, Shigella, and Ureoplasma, qui contient tous des espèces potentiellement pathogènes, étaient présentes en plus fortes proportions chez les femmes atteintes d’endométriose de stade 3 et 4.
Par ailleurs, il semblerait également que l’endométriose affecte la qualité du microbiote. Ainsi, l’endométriose semble être associée avec une présence accrue de Proteobacterie, Enterobacteriaceae, Streptococcus spp. and Escherichia coli dans les différents endroits comprenant un microbiome. Le phylum Firmicutes and la genus Gardnerella semblent aussi être impliquées mais cela reste à confirmer.
L’interaction entre endométriose et microbiote serait donc bidirectionnelle[5].
Focus sur les liens entre microbiote intestinal et endométriose
De plus en plus de recherches mettent en évidence le lien entre l’altération du microbiote intestinal et le développement de maladies hormono-dépendantes telles que l’endométriose (mais aussi le syndrome des ovaires polykystiques, l’ostéoporose, certains cancers du sein, etc.). Il semblerait qu’en prenant soin de son microbiote intestinal et en évitant ainsi la dysbiose, on pourrait prévenir et potentiellement atténuer ces maladies.
Sur l’endométriose, les chiffres parlent d’eux-mêmes : 90 % des femmes atteintes d’endométriose présenteraient des symptômes digestifs/gastro-intestinaux[6].
Deux études, l’une menée en Suède[7] et l’autre à Shangaï[8] se sont penchées sur le lien entre le microbiote intestinal et l’endométriose. Ces études portent plusieurs conclusions :
- la diversité des flores intestinales des patientes atteintes d’endométriose se révélait inférieure à celle des patientes témoins
- les abondances des bactéries différaient. Ainsi, dans l’étude chinoise, Prevotella dominait parmi les malades, tandis que Coprococcus s’imposait chez les témoins
- certaines fonctions microbiennes (traitement de l’information environnementale, système endocrinien et système immunitaire) étaient plus développées chez les patientes atteintes d’endométriose
- Les taux d’hormones, et notamment d’œstrogènes, et de facteurs inflammatoires étaient significativement plus élevés chez les femmes souffrant d’endométriose.
- des corrélations ont été détectées entre l’abondance de Blautia et Dorea et le niveau d’oestrogènes, et entre l’abondance de Subdoligranulum et le niveau de facteurs inflammatoires.
Microbiote intestinal et taux d’œstrogènes : une relation à double sens
Le microbiote intestinal comprend un ensemble de bactéries qui ont la capacité d’affecter la quantité d’oestrogènes circulant dans notre corps. C’est que l’on appelle l’estrobolome. Ainsi, l’estrobolome, et notamment les Ruminococcaceae et les Clostridia, pourrait affecter les taux d’œstrogènes circulant dans le sang, en modulant la réabsorption des œstrogènes excrétés dans la bile qui finissent par pénétrer dans l’intestin.
L’endométriose étant une maladie hormono-dépendante dont les lésions évoluent, se développent et grossissent sous l’effet des œstrogènes, il est facile de comprendre qu’un microbiote intestinal en mauvais état, faisant fortement augmenter le taux d’estrobolome, pourra moins facilement métaboliser les œstrogènes et donc jouer moins correctement son rôle de régulation du taux d’œstrogènes dans le sang – contribuant ainsi une activation plus importante des lésions d’endométriose dans un contexte d’hyper-oestrogénie[9].
| Explication scientifique de la métabolisation des œstrogènes et du lien avec le microbiote Une partie des œstrogènes sont éliminés par les selles, la bile ou l’urine après avoir été métabolisés par le foie, par le biais d’un processus appelé « glucurono-conjugaison » qui rend les œstrogènes solubles dans l’eau et donc éliminables par le corps. Le processus inverse, la « déconjugaison », va lui pouvoir réactiver les œstrogènes excrétés par la bile. Ils deviendront alors des « œstrogènes libres » (les œstrogènes les plus actifs) qui pourront être réabsorbés dans le tube digestif et remis en circulation dans le sang. Ce recyclage des œstrogènes usés est normal et fait partie de l’écosystème incroyable de notre corps qui va réguler la quantité d’hormones circulantes en fonction de ses besoins. Mais cet équilibre subtil est tributaire d’une enzyme, la bêta-glucuronidase, elle-même dépendante de notre microbiote intestinal et de la quantité de bactéries dites « estrobolomes ». En effet, trop de bactéries estrobolomes augmente la quantité d’œstrogènes circulants (l’inverse est aussi vrai). Ainsi, les dysbioses digestives telles que les candidoses, la prolifération bactérienne gastrique excessive ou encore la prolifération de lipopolysaccharides ou de bactéries Gram négatif peuvent faire proliférer les bactéries dites « estrobolomes » et trop augmenter le niveau d’œstrogènes circulants. |
Le microbiote intestinal jouerait un rôle dans le développement, l’évolution et la progression de l’endométriose
De nombreuses études scientifiques ont montré qu’il est possible que la flore intestinale soit impliquée dans le déclenchement et la progression de l’endométriose[10]. Ainsi, le fait de se supplémenter avec la bonne souche de probiotiques a une action sur l’évolution de la maladie. Cela permet de faire diminuer le nombre et le volume des lésions d’endométriose.
Cette souche bactérienne stimulerait en effet l’activité de certaines cellules issues du système immunitaire, permettant ainsi d’éliminer naturellement les cellules anormales dans le corps et particulièrement celles constituant les lésions d’endométriose.
Le microbiote intestinal jouerait un rôle sur les douleurs ressenties
Selon une étude qui date de 2011[11], l’amélioration du microbiote intestinal grâce à cette même souche de probiotiques permettrait de réduire significativement les douleurs ressenties, notamment durant les règles, par les femmes atteintes d’endométriose (en comparaison de femmes traitées avec un placebo).
Le microbiote joue un rôle dans la diffusion et la régulation de l’inflammation
D’autres recherches évoquent le rôle régulateur du microbiote intestinal dans les processus inflammatoires en dehors du système digestif.
L’inflammation est une des réactions immunitaires normales du corps en présence d’éléments pathogènes. Etant donné que l’intestin contient 70 % des cellules immunitaires du corps humain, il joue un rôle très important dans la régulation de l’inflammation.
Dans le cadre de l’endométriose, il semblerait que la toxine lipopolysaccharide, issue des bactéries Gram négatif de l’intestin (notamment l’Escherichia coli) soit impliquée, conjointement à l’œstradiol, dans l’inflammation pelvienne et le développement et la croissance de l’endométriose[12]. Ainsi, le lipopolysaccharide régule la réponse pro-inflammatoire dans le bassin et la croissance de l’endométriose via la cascade LPS/TLR4. Cette étude a montré que le sang menstruel était fortement contaminé par Escherichea coli et les échantillons endométriaux étaient colonisés par d’autres microbes. Une interférence entre l’inflammation et les stéroïdes ovariens ou la réaction de stress a également été observée dans le bassin. Le traitement par GnRH aggrave encore la colonisation microbienne intra-utérine, avec pour conséquence l’apparition d’endométrites chez les femmes atteintes d’endométriose.
Par ailleurs, les femmes atteintes d’endométriose sont plus sujettes aux problèmes d’inflammation intestinale que celles n’étant pas atteintes de la maladie[13].

Un guide accessible et digeste afin de vous informer sur ce symptôme très peu abordé par la médecine allopathique et complémentaire :
- de nombreuses clés de compréhension de ce symptôme multifactoriel
- une feuille de route pour agir dès aujourd’hui grâce à des outils simples et efficaces
Le guide de l’Endobelly : En comprendre les causes et agir pour se réconcilier avec son ventre
Vous avez déjà ressenti un ou plusieurs de ces symptômes :
- Gonflement important du ventre
- Ventre dur
- Ventre douloureux ou inconfortable
- Ballonnements
- Perte d’appétit
- Nausées
- Crampes abdominales
- Constipation
- Diarrhées
- Mouvements intestinaux douloureux
- Vertiges
- Vomissements
Plusieurs jours par mois, vous ne savez plus comment vous habiller car soit vos vêtements sont très inconfortables, soit ils sont tout simplement impossibles à enfiler.
On vous a déjà demandé si vous étiez enceinte de 4 voire 6 mois alors que vous étiez malheureusement en pleine crise d’endométriose ou d’endobelly.
Vous n’avez pas été prise au sérieux par les experts à qui vous avez parlé de ce symptôme que vous reliez à l’endométriose, qui est souvent peu reconnu et pour lequel il n’y a soi-disant pas de solution.
L’inflammation intestinale : le milieu idéal pour développer facilement une candidose
La candidose intestinale résulte de la prolifération désordonnée d’un champignon, le Candida albicans, normalement présent dans le corps humain.
Son développement incontrôlé constitue une menace toxique pour le fonctionnement du corps humain. Il est la plupart du temps le résultat d’une mauvaise alimentation et d’une utilisation excessive d’antibiotiques.
L’inflammation intestinale peut également favoriser le développement d’une candidose dans la mesure où l’inflammation perturbe l’équilibre des micro-organismes vivant dans le tube digestif[14]. Sans bactéries favorables, la levure Candida est capable de dominer rapidement son environnement et de coloniser d’autres zones du corps comme le vagin, provoquant des infections vaginales, de type mycose, à répétition.
Certains médecins pensent en outre que la prolifération du candida albicans aurait un lien avec l’apparition et la progression de l’endométriose.
Certaines femmes qui reconnaissent que certains de leurs symptômes sont liés à cette levure et qui engagent les actions nécessaires pour surmonter la profilération de la levure, ont été capables d’inverser les symptômes de l’endométriose. Le traitement du candida inclut l’utilisation d’agents qui tuent la levure, des modifications alimentaires et des probiotiques afin de rétablir une flore saine dans le système gastro-intestinal[15] et [16].
Les contraceptions hormonales sont en général le premier traitement prescrit pour soulager les douleurs d’endométriose. Cependant, ils ne soulagent pas toujours les douleurs et ils ont été identifiés comme un contributeur significatif à la prolifération du champignon.
Focus sur les liens entre microbiote gynécologique et endométriose
Tout comme l’altération du microbiote intestinal contribuerait au développement et aux symptômes de l’endométriose, l’altération du microbiote gynécologique serait également un contributeur du développement de l’endométriose.
Selon une étude datant de 2020[17], les femmes atteintes d’endométriose seraient davantage victimes de dysbiose (altération du microbiote) tout au long de leur appareil reproducteur et certaines bactéries seraient ainsi responsables du développement de l’endométriose.
Le microbiote vaginal serait un outil prédictif de sévérité de l’endométriose
Selon une étude[18] qui date de 2020, l’analyse de la flore vaginale permettrait de déterminer la gravité et de la sévérité de l’endométriose chez la femme. Dans le cadre de cette étude, la bactérie Anaerococcus était davantage retrouvée lors des menstruations chez les femmes atteintes d’une forme sévère de la maladie que chez celles touchées par des formes moins avancées.
Le microbiote utérin influencerait la réussite des procédures de fécondation in vitro
Le microbiote vaginal, le microbiote cervical et le microbiote utérin sont tous différents. Le microbiote utérin, et particulièrement la présence de bactéries Lactobacillus crispatus, aurait même une influence sur la réussite d’une grossesse après implantation d’embryons issus de fécondation in vitro (FIV), d’après les résultats d’une étude qu’il a dirigée dans une clinique de fertilité espagnole, publiés dans la revue American Journal of Obstetrics and Gynecology.
Cette information concerne toutes les femmes en procréation médicalement assistée. Cependant, il est connu que la résistance à la progestérone est un élément de la physiopathologie de l’endométriose et que celle-ci peut modifier la flore vaginale. L’infertilité (probablement induite par le stress oxydatif et l’inflammation) est présente chez bon nombre de femmes atteintes d’endométriose, alors un traitement par probiotiques spécifiques pourrait être envisagé.

Un guide accessible et digeste afin de vous informer sur ce symptôme très peu abordé par la médecine allopathique et complémentaire :
- de nombreuses clés de compréhension de ce symptôme multifactoriel
- une feuille de route pour agir dès aujourd’hui grâce à des outils simples et efficaces
Le guide de l’Endobelly : En comprendre les causes et agir pour se réconcilier avec son ventre
Vous avez déjà ressenti un ou plusieurs de ces symptômes :
- Gonflement important du ventre
- Ventre dur
- Ventre douloureux ou inconfortable
- Ballonnements
- Perte d’appétit
- Nausées
- Crampes abdominales
- Constipation
- Diarrhées
- Mouvements intestinaux douloureux
- Vertiges
- Vomissements
Plusieurs jours par mois, vous ne savez plus comment vous habiller car soit vos vêtements sont très inconfortables, soit ils sont tout simplement impossibles à enfiler.
On vous a déjà demandé si vous étiez enceinte de 4 voire 6 mois alors que vous étiez malheureusement en pleine crise d’endométriose ou d’endobelly.
Vous n’avez pas été prise au sérieux par les experts à qui vous avez parlé de ce symptôme que vous reliez à l’endométriose, qui est souvent peu reconnu et pour lequel il n’y a soi-disant pas de solution.
Comment prendre soin de son microbiote quand on est atteinte d’endométriose ?
Le microbiote humain se constitue à la naissance et se stabilise pendant nos premières années de vie.
Plusieurs facteurs impactent son équilibre et sa diversité :
- le mode d’accouchement(par voie basse ou par césarienne)
- l’alimentation dans les premiers mois de vie (allaitement maternel ou lait maternisé)
- le patrimoine génétique
- le type d’alimentation
- l’exposition aux perturbateurs endocriniens et aux toxines
- la prise de certains médicaments, dont la pilule, les antibiotiques et les anti-inflammatoires non stéroïdiens
- le stress
Une alimentation adaptée pour réduire voire faire disparaître la dysbiose
Aujourd’hui, notre alimentation est particulièrement inadaptée pour maintenir un microbiote en bonne santé : alimentation très transformée, riche en sucre, riche en additif, pauvre en fibres, etc.
La diversité du microbiote humain s’est appauvrie de manière drastique ces dernières années en raison de notre façon de nous alimenter.
En modifiant l’alimentation, l’idée est de nourrir les bonnes bactéries (les probiotiques) présentes dans l’intestin et d’augmenter leur quantité afin qu’elles prennent la place des mauvaises. Pour nourrir les bonnes bactéries, il faut leur apporter des prébiotiques. On trouve les probiotiques et les prébiotiques dans l’alimentation du quotidien d’où le rôle fondamental d’une alimentation adaptée pour soigner son endométriose.
Sur le sujet de l’alimentation, de son impact sur l’endométriose par le biais du microbiote et des conseils à mettre en place, je vous invite à aller lire mon article dédié : Comment votre alimentation et votre digestion influencent l’endométriose dont vous êtes atteinte ?
Se supplémenter avec une souche précise : le Lactobacillus Gasseri
En complément d’une alimentation équilibrée, il est possible de se supplémenter avec une souche probiotique spécifique adaptée : le Lactobacillus gasseri. En effet, une étude expérimentale[19] a montré que le probiotique Lactobacillus gasseri pouvait intervenir dans la régression de l’endométriose en faisant diminuer le nombre et le volume des lésions et en réduisant les douleurs lors des menstruations.
La souche Lactobacillus gasseri pourrait également être utile en cas de syndrome de l’intestin irritable avec diarrhée, qui sont des symptômes récurrents trouvés couramment chez les femmes atteintes d’endométriose.
Faire appel à la naturopathie et à la phyto-aromathérapie
Une fois une dysbiose mise en évidence par une analyse des selles ou un examen clinique, il existe plusieurs protocoles à mettre en place en naturopathie et en phyto-aromathérapie pour assainir le terrain. Ils font une large place aux huiles essentielles : huile d’origan, acide caprylique, extrait de pépins de pamplemousse, mais aussi des huiles essentielles à visée antifongique, etc.
[1] Baris Ata, Sule Yildiz, Engin Turkgeldi, Vicente Pérez Brocal, EnerCagri Dinleyici, Andrés Moya & Bulent Urman, The Endobiota Study: Comparison of Vaginal, Cervical and Gut Microbiota Between Women with Stage 3/4 Endometriosis and Healthy Controls
[2] Chen C et al. The microbiota continuum along the female reproductive tract and its relation to uterine-related diseases. Nature Communications 8, Article number: 875 (2017).
[3] Idem
[4] Baris Ata, Sule Yildiz, Engin Turkgeldi, Vicente Pérez Brocal, EnerCagri Dinleyici, Andrés Moya & Bulent Urman, The Endobiota Study: Comparison of Vaginal, Cervical and Gut Microbiota Between Women with Stage 3/4 Endometriosis and Healthy Controls
[5] Leonardi M, Hicks C, El-Assaad F, El-Omar E, Condous G. Endometriosis and the microbiome: a systematic review. BJOG. 2020 Jan;127(2):239-249. doi: 10.1111/1471-0528.15916. Epub 2019 Sep 19. PMID: 31454452.
[6] MAROUN P , COOPER M., REID G., KEIRSE M., Relevance of gastrointestinal symptoms in endometriosis, 29 July 2009, https://doi.org/10.1111/j.1479-828X.2009.01030.x
[7] Svensson A, Brunkwall L, Roth B et al. Associations Between Endometriosis and Gut Microbiota. Reprod Sci. 2021 Mar 3. doi: 10.1007/s43032-021-00506-5.
[8] Shan J, Ni Z, Cheng W et al. Gut microbiota imbalance and its correlations with hormone and inflammatory factors in patients with stage 3/4 endometriosis. Arch Gynecol Obstet. 2021 Apr 11.
[9] Mary E Salliss, Leslie V Farland, Nichole D Mahnert, Melissa M Herbst-Kralovetz, The role of gut and genital microbiota and the estrobolome in endometriosis, infertility and chronic pelvic pain, Human Reproduction Update, 2021; dmab035
[10] Laschke, Menger, The gut microbiota: a puppet master in the pathogenesis of endometriosis? Am J Obstet Gynecol. 2016 Jul
[11] Itoh H, Sashihara T, Hosono A, Kaminogawa S, Uchida M. Lactobacillus gasseri OLL2809 inhibits development of ectopic endometrial cell in peritoneal cavity via activation of NK cells in a murine endometriosis model. Cytotechnology. 2011 Mar;63(2):205-10. doi: 10.1007/s10616-011-9343-z. Epub 2011 Mar 16. PMID: 21409454; PMCID: PMC3080482.
[12] Khan KN, Kitajima M, Inoue T, Fujishita A, Nakashima M, Masuzaki H. 17β-estradiol and lipopolysaccharide additively promote pelvic inflammation and growth of endometriosis. Reprod Sci. 2015;22(5):585-594. doi:10.1177/1933719114556487
[13] K Ballard, et al. Endometriosis and irritable bowel syndrome: co-morbidity or misdiagnosis?. BJOG: An International Journal of Obstetrics & Gynaecology. 2009; 116: 129–130.
[14] T Jess, et al. Increased risk of inflammatory bowel disease in women with endometriosis: a nationwide Danish cohort study. Gut. 2011 Dec 19. [Epub ahead of print]
[15] TR Nichols, et al. The association of atopic diseases with endometriosis. Ann Allergy. 1987 Nov; 59 (5): 360-363.
[16] K Lamb, et al. Endometriosis: a comparison of associated disease histories. Am J Prev Med. 1986 Nov-Dec; 2 (6): 324-329.
[17] Wei W, Zhang X, Tang H et al. Microbiota composition and distribution along the female reproductive tract of women with endometriosis. Ann Clin Microbiol Antimicrob. 2020 Apr 16;19(1):15. doi: 10.1186/s12941-020-00356-0
[18] Perrotta AR, Borrelli GM, Martins CO, et al. The Vaginal Microbiome as a Tool to Predict rASRM Stage of Disease in Endometriosis: a Pilot Study. Reprod Sci. 2020;27(4):1064–1073. doi:10.1007/s43032-019-00113-5
[19] Laschke, Menger, The gut microbiota: a puppet master in the pathogenesis of endometriosis? Am J Obstet Gynecol. 2016 Jul)
Itoh H, Uchida M, Sashihara T, Ji ZS, Li J, Tang Q, Ni S, Song L, Kaminogawa S. Lactobacillus gasseri OLL2809 is effective especially on the menstrual pain and dysmenorrhea in endometriosis patients: randomized, double-blind, placebo-controlled study. Cytotechnology. 2011 Mar;63(2):153-61. doi: 10.1007/s10616-010-9326-5. Epub 2010 Dec 10. PMID: 21153437; PMCID: PMC3080472.
Itoh H, Uchida M, Sashihara T, Ji ZS, Li J, Tang Q, Ni S, Song L, Kaminogawa S. Lactobacillus gasseri OLL2809 is effective especially on the menstrual pain and dysmenorrhea in endometriosis patients: randomized, double-blind, placebo-controlled study. Cytotechnology. 2011 Mar;63(2):153-61. doi: 10.1007/s10616-010-9326-5. Epub 2010 Dec 10. PMID: 21153437; PMCID: PMC3080472.



6 commentaires
Alexa
Extraordinaire… Enfin de vraies avancées sur ce sujet. Atteinte d’endo ma vie n’est faite que de limites, avec ces recherches cela offre de l’espoir.
Merci à la ou aux personne(s) ayant créé ce site.
Bertille
Bonjour Alexa,
merci pour votre message ! J’espère que vous allez trouver des solutions pour mieux vivre avec l’endométriose. Belle journée
Emilie
Bonjour ! Atteinte d’endométriose découverte il y a 6 ans, je me documente énormément et c’est pourtant le premier article aussi complet que je lis qui fait le lien entre le microbiote intestinal et l’endométriose. Je vais tenter de me supplémenter avec cette souche afin de voir si une amélioration se profile. Enfin un espoir ! Merci infiniment.
Bertille
Merci Emilie pour votre commentaire. Il me tient à cœur de comprendre ces mécanismes et ensuite d’expliquer et de transmettre pour nous aider toutes sur ce chemin avec la maladie.
Clée
Waouw, mille merci pour ton article sur le sujet, je l’ai trouvé très très complet et pourtant j’avais déjà potassé pas mal d’études. Celles que j’ai lu sur le L-Gasseri sont assez controversées parce qu’il n’y a pas un pannel de testeurs assez grands pour qu’elle soit fiable et il me semble que la plupart avaient des conflits d’intérêts. Bref, je découvre tout ça pas à pas et j’ai adoré ton article, très complet et très intéressant !
Je vais commencer à lire davantage ton blog qui a l’air d’être une mine d’or !
Bertille
Merci Clée pour ton message ! Je trouve toutes ces recherches passionnantes et transmettre l’information encore plus !